La ciencia mendocina avanza para frenar el Chagas: diagnóstico temprano y nuevos tratamientos
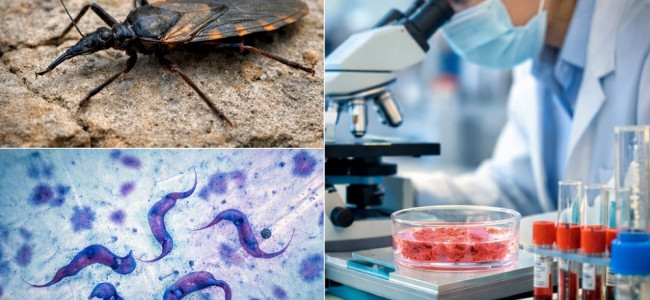
Se trata de investigaciones del Instituto de Histología y Embriología de Mendoza. Uno de los trabajos ya tiene aplicación en el sistema de salud para detectar la enfermedad de manera rápida en personas recién nacidas. El otro avanza en el desarrollo de estrategias terapéuticas para atacar al parásito sin dañar células humanas.

Investigadoras del IHEM-Conicet-UNCUYO trabajan sobre dos líneas centrales para abordar la enfermedad de Chagas. Foto: Unidiversidad
El Chagas continúa siendo un problema sanitario en América Latina y Argentina. Según la Organización Panamericana de la Salud (OPS), afecta a unos 6 millones de personas en la región y provoca alrededor de 12.000 muertes anuales. Actualmente, la transmisión congénita representa uno de los principales desafíos. En nuestro país, se calcula que cada año nacen cerca de 1500 bebés con esta enfermedad. Esta vía de transmisión es especialmente sensible porque la mayoría de los recién nacidos no presenta síntomas. Si no son diagnosticados y tratados a tiempo, pueden avanzar hacia etapas crónicas de la enfermedad durante la adolescencia o la adultez, lo que compromete su salud y aumenta las posibilidades de nuevos casos por contagios de madre a hijo o hija durante el embarazo o el parto.
En este contexto, la investigación científica cumple un rol clave para comprender mejor la enfermedad, optimizar los métodos de diagnóstico y desarrollar nuevas estrategias terapéuticas. En Mendoza, investigadoras del IHEM-Conicet-UNCUYO trabajan sobre dos líneas centrales para abordar la enfermedad de Chagas.
 Equipo de investigación. De Der a Izq: Patricia Romano, María Belén López, María Cristina Vanrell y Gabriel Ferri. Foto: Unidiversidad
Equipo de investigación. De Der a Izq: Patricia Romano, María Belén López, María Cristina Vanrell y Gabriel Ferri. Foto: Unidiversidad
Uno de los estudios, encabezado por Patricia Romano, directora del Laboratorio de Biología del Trypanosoma cruzi y enfermedad de Chagas, apunta al diagnóstico molecular temprano del Chagas congénito mediante la detección directa del ADN del Trypanosoma cruzi en sangre de recién nacidos. El avance de su equipo permite evitar esperas de seis a diez meses para confirmar la infección por serología y abre la posibilidad de iniciar el tratamiento en los primeros meses de vida, cuando la eficacia puede acercarse al 99 % o al 100 %. El objetivo es cortar una cadena de transmisión intergeneracional que puede pasar de madre a hija y luego a nuevos hijos si no se detecta a tiempo.
Este trabajo se articula con las políticas sanitarias vinculadas a la estrategia ETMI Plus (Eliminación de la Transmisión Materno-infantil) de la OPS, que busca justamente eliminar la transmisión materno-infantil de VIH, sífilis, hepatitis B y Chagas. En Mendoza, se conformó la mesa de gestión provincial de la ETMI Plus que reúne a las áreas de atención materno-infantil, vigilancia epidemiológica, laboratorio, atención primaria y hospitales, con el objetivo de mejorar el diagnóstico de estas enfermedades, sus tratamientos, registros y el seguimiento de personas gestantes y recién nacidos.
“La eliminación de la enfermedad de Chagas como problema de salud pública requiere situar a las mujeres en el centro de las estrategias de diagnóstico, tratamiento y atención”, enfatizó el doctor Jarbas Barbosa, director de la OPS. La integración de tamizaje materno-infantil, el fortalecimiento de la atención primaria y la promoción de políticas sensibles al género son acciones que, según la OPS y la Coalición Global de Chagas, resultan fundamentales para reducir la transmisión congénita y el impacto social y sanitario de la enfermedad.

Doctora Patricia Barrera y equipo. Foto: Unidiversidad
El otro estudio investiga nuevas estrategias terapéuticas contra el Trypanosoma cruzi. La investigadora Patricia Barrera y su equipo trabajan sobre compuestos capaces de atacar diferencias biológicas del parásito respecto de las células humanas: una línea estudia lactonas sesquiterpénicas, moléculas naturales que generan estrés oxidativo en el parásito; otra analiza la posibilidad de interferir en la síntesis de ergosterol, un componente clave de su membrana. La idea es avanzar hacia tratamientos más selectivos, capaces de dañar al microorganismo sin afectar de manera significativa las células del paciente.
Estas investigaciones todavía tienen distintos grados de desarrollo: el diagnóstico molecular temprano ya muestra una aplicación en campo concreta, mientras que las nuevas terapias permanecen en fase de laboratorio. Sin embargo, ambas líneas apuntan a transformar el conocimiento científico en herramientas útiles para el sistema de salud.
Del nacimiento al laboratorio: por qué detectar antes cambia todo
En el caso del diagnóstico temprano, Romano explicó que el punto de partida fue una investigación básica sobre la interacción entre el Trypanosoma cruzi y la célula hospedadora. Sin embargo, los resultados fueron empujando al equipo hacia una medicina más traslacional, orientada a llevar hallazgos del laboratorio a una aplicación concreta para la población. Ese giro terminó de consolidarse hacia 2020, cuando, junto a la especialista Cristina Vanrell, presentaron un proyecto para analizar factores de riesgo asociados a la transmisión congénita, que es la forma de contagio más frecuente hoy en día.
La transmisión vectorial, por contacto con las heces o la orina infectadas de vinchucas, pudo ser mejor controlada en muchas zonas a través de fumigaciones y otras estrategias sanitarias, pero la transmisión congénita, de madre a hijo o hija durante el embarazo, siguió planteando otro tipo de dificultad. “El problema no era solo clínico. También era temporal. Hasta hace no mucho, en muchos casos el diagnóstico del recién nacido debía esperar entre seis y diez meses para poder confirmarse por serología, es decir, detectando anticuerpos propios del bebé. Esa espera abría una ventana demasiado amplia. La madre tenía que regresar meses después al sistema de salud con su hijo, sostener controles, no perder el seguimiento y lograr que el caso no se diluyera en el camino. En ese intervalo, muchas oportunidades podían perderse”, afirmó la investigadora.

Romano explicó que el punto de partida fue una investigación básica sobre la interacción entre el Trypanosoma cruzi y la célula hospedadora. Foto: Unidiversidad
La respuesta que empezó a construir el equipo mendocino fue el diagnóstico molecular. En vez de aguardar a que la persona recién nacida produzca anticuerpos detectables, el método permite buscar directamente el ADN del parásito en sangre. “La diferencia es de fondo. Ya no se trata de esperar una reacción inmunológica posterior, sino de identificar la presencia del Trypanosoma cruzi desde el comienzo”, remarcó Romano.
Ese cambio de enfoque no surgió como una idea abstracta. Se fue imponiendo a partir de los propios resultados del estudio y de una necesidad cada vez más visible en terreno. El grupo logró poner a punto el sistema y montar un servicio tecnológico de alto nivel para recibir muestras y procesarlas. Durante el proyecto, trabajaron con el Hospital Perrupato, en San Martín, y también recibieron muestras del Hospital Lagomaggiore. Esa red permitió validar la estrategia y darle una proyección sanitaria concreta.
La importancia del avance también encontró eco en el plano institucional. Según relató Romano, los resultados fueron presentados al Ministerio de Salud de Mendoza y, a partir de ese proceso, en septiembre de 2024 se dictó una resolución para implementar el diagnóstico molecular en hospitales públicos con servicio de obstetricia, como el Lagomaggiore. “El punto central nunca fue que el estudio se hiciera exclusivamente en el laboratorio, sino que se hiciera masivo, que se incorporara como práctica. Que la evidencia acumulada se tradujera en una decisión sanitaria”, detalló la especialista.
El argumento detrás de esa insistencia fue contundente: cuando un recién nacido o recién nacida recibe tratamiento temprano, la eficacia de curación ronda el 99 %. En ese dato se condensa el peso real del diagnóstico precoz. “No se trata solo de mejorar estadísticas ni de perfeccionar técnicas de laboratorio. Se trata de modificar el pronóstico de un bebé desde el inicio de su vida”, resaltó.
 La enfermedad de Chagas, causada por el parásito Trypanosoma cruzi, se transmite principalmente por las heces de la vinchuca (insecto vector) al picar. Foto: Unidiversidad
La enfermedad de Chagas, causada por el parásito Trypanosoma cruzi, se transmite principalmente por las heces de la vinchuca (insecto vector) al picar. Foto: Unidiversidad
Además, el impacto positivo de esta investigación excede los casos individuales. Romano remarcó que la transmisión congénita tiene una lógica silenciosa pero persistente. “Una madre con infección puede transmitirla a su hija al nacer. Si esa niña no es diagnosticada ni tratada, puede llegar a la adultez y transmitirla a su vez a sus hijos. Es una cadena intergeneracional”, dijo. En el trabajo de campo, ese patrón aparecía incluso en las conversaciones dentro de los hospitales: madres con recién nacidos infectados que estaban acompañadas por sus propias madres, quienes también relataban tener Chagas. “Cortar esa secuencia en el nacimiento no solo cura a un niño, también interrumpe una vía de transmisión que puede prolongarse durante generaciones”, indicó.
Romano también aportó una aclaración importante para leer los datos con cuidado. Cuando empezaron a aplicar el diagnóstico molecular, encontraron un porcentaje algo mayor de infecciones en menores respecto de registros previos. “Eso no implica necesariamente que hayan aumentado los casos, sino que cambió la sensibilidad del método. El sistema usado antes en recién nacidos, basado en la visualización directa del parásito al microscopio, dependía mucho de quien observaba la muestra y tenía una sensibilidad relativamente baja. La nueva técnica encuentra más casos porque busca mejor”, manifestó la investigadora del IHEM. Por eso, advierte que no es correcto comparar porcentajes obtenidos con herramientas distintas como si describieran una misma realidad sin matices.
Para Romano, el trabajo abre, además, otra puerta relevante: el seguimiento en etapas crónicas. En personas adultas, la serología sigue siendo una herramienta sensible para confirmar la infección, pero, cuando se quiere evaluar la respuesta al tratamiento, el panorama cambia. “Los anticuerpos no descienden rápido y no reflejan de inmediato si la carga parasitaria bajó. Allí el diagnóstico molecular vuelve a aparecer como una herramienta útil, aunque con una exigencia técnica mayor, porque, en la fase crónica, la cantidad de parásito en sangre es mucho más baja. Optimizar esa sensibilidad es parte de lo que viene”, señaló.

Patricia Barrera, investigadora del instituto, desarrolla dos proyectos que parten de una misma pregunta: qué diferencias biológicas presenta el Trypanosoma cruzi respecto de las células humanas y cómo aprovechar esas diferencias para golpearlo con precisión. Foto: Unidiversidad
Cómo atacar al parásito sin dañar al paciente
Mientras una parte del equipo trabaja sobre diagnóstico y aplicación clínica temprana, otra línea del IHEM avanza en un problema igual de estructural: la necesidad de mejorar los tratamientos que deben seguir las personas contagiadas con Chagas. Patricia Barrera, investigadora del instituto, desarrolla dos proyectos que parten de una misma pregunta: qué diferencias biológicas presenta el Trypanosoma cruzi respecto de las células humanas y cómo aprovechar esas diferencias para golpearlo con precisión.
Según Barrera, la enfermedad de Chagas tiene una particularidad que explica buena parte de su gravedad. El parásito infecta células de mamíferos y muestra una marcada afinidad por los cardiomiocitos, las células del corazón. De allí surge una de las formas más severas de la enfermedad: la cardiomiopatía chagásica. El daño puede ir alterando el funcionamiento cardíaco hasta volverse irreversible. Frente a eso, la especialista plantea una estrategia concreta: no atacar de manera indiscriminada, sino encontrar puntos débiles del parásito que no estén presentes o no funcionen igual en las células humanas.
Una de las líneas surgió a partir de una colaboración con químicos de la Universidad Nacional de San Luis, que enviaron compuestos naturales purificados de plantas. “Entre ellos, un grupo de moléculas llamó la atención: las lactonas sesquiterpénicas. Estos compuestos mostraron actividad contra el Trypanosoma cruzi, y eso llevó al equipo a estudiar con más detalle qué estaba pasando”, detalló.
Lo que se observó fue un fenómeno de estrés oxidativo. En otras palabras, una descompensación interna que genera moléculas dañinas y termina afectando al parásito. “La clave está en que el Trypanosoma cruzi posee una maquinaria antioxidante diferente de la de las células de mamíferos. Más simple, menos sofisticada. Esa diferencia ofrece un blanco terapéutico. Si se golpea esa vía de defensa, el parásito queda expuesto a un daño que ya no puede compensar igual que una célula humana”, remarcó Barrera.

“Con dosis menores, ya es posible matar al parásito sin generar el mismo impacto sobre la célula hospedadora", dijo Barrera. Foto: Unidiversidad
La investigadora, además, destacó un dato que resulta central para cualquier desarrollo farmacológico: aunque en dosis elevadas estos compuestos podían afectar también células sanas de mamíferos, no hacía falta llegar a ese punto. “Con dosis menores, ya es posible matar al parásito sin generar el mismo impacto sobre la célula hospedadora. Ese margen es el que vuelve prometedora la línea de investigación. No alcanza con que una sustancia mate al agente infeccioso; tiene que hacerlo sin convertirse en un problema mayor para el paciente”, manifestó.
La segunda línea del equipo de Barrera se apoya en otra diferencia biológica del Trypanosoma cruzi. Mientras las células humanas usan colesterol en sus membranas, el parásito utiliza ergosterol. Esa singularidad permite pensar en otro punto vulnerable. Si se interfiere la síntesis de ergosterol, se compromete la estabilidad de la membrana del microorganismo. A partir de esa idea, el grupo decidió avanzar sobre una estrategia de polifarmacología: combinar un compuesto que altere la vía antioxidante del ergosterol. La lógica es presionar al parásito sobre dos flancos al mismo tiempo, dificultando sus posibilidades de adaptación.
Ese razonamiento no es menor. “Los microorganismos suelen desplegar mecanismos de escape. Si una vía se bloquea, intentamos someterla por otra. Combinar blancos terapéuticos puede reducir esa capacidad de respuesta. Y allí aparece otro elemento atractivo del proyecto: algunos de los compuestos que interfieren en la síntesis de ergosterol ya existen y se usan en el mercado. Eso abre la puerta al reposicionamiento de drogas, una estrategia que busca reutilizar compuestos conocidos para nuevas indicaciones terapéuticas. La ventaja es clara: cuando una droga ya circula o está aprobada, parte del recorrido en materia de seguridad y conocimiento farmacológico ya fue hecho”, dijo Barrera.
De todos modos, la especialista aclara que el trabajo todavía está en fase de laboratorio. “El recorrido es largo y tiene filtros estrictos. Primero se estudia el efecto sobre el parásito aislado. Luego hay que pasar a situaciones más complejas, en las que el Trypanosoma cruzi ya infectó una célula. Ese paso es decisivo, porque muchas sustancias funcionan bien en cultivos simples, pero fallan cuando deben actuar dentro de una célula sin destruirla. Ya estamos en ensayos y modelos animales, como ratones, y recién más adelante podría pensarse en etapas preclínicas más avanzadas”, explicó.
Romano pidió que se evite la expresión “mal de Chagas”, por su carga estigmatizante. Foto: Unidiversidad
Ciencia aplicada, nuevos tratamientos
El telón de fondo de esta investigación es el límite de las terapias actuales. Barrera recordó que los compuestos usados hoy contra el Chagas, como benznidazol y nifurtimox, arrastran décadas de utilización. “Son valiosos, sobre todo cuando la infección se detecta temprano, especialmente en niños, pero también muestran restricciones, sobre todo en etapas más tardías. Es que muchas personas no saben cuándo se infectaron, transitan fases sin síntomas claros o llegan al diagnóstico cuando el parásito ya siguió otro curso dentro del organismo”, sostuvo la investigadora.
Por eso, los trabajos del IHEM pueden leerse como una intervención sobre dos cuellos de botella. Uno busca acortar el tiempo del diagnóstico, especialmente en el Chagas congénito. El otro, ampliar y mejorar el arsenal terapéutico disponible para el futuro. En ambos casos, la ciencia se mueve con tiempos que no son los del anuncio fácil. Nada de esto está cerrado, nada puede presentarse como una solución definitiva, pero sí hay avances visibles: el conocimiento científico se vuelca al sistema de salud y, al mismo tiempo, genera nuevas hipótesis para tratamientos más selectivos.
“En una enfermedad donde, durante años, el atraso se midió en meses, en tratamientos limitados y en silencios heredados. Ese conjunto de avances no resuelve todo, pero empieza a cambiar algo importante: la dirección”, concluyó Barrera.
No es “mal de Chagas”
Romano pidió que se evite la expresión “mal de Chagas”, por su carga estigmatizante. No es una cuestión de corrección superficial. La forma de nombrar también ordena la percepción social del problema. “Tener infección por Trypanosoma cruzi no equivale automáticamente a desarrollar una patología cardíaca ni a quedar impedido para trabajar. De hecho, solo cerca del 30 % de las personas infectadas desarrolla manifestaciones patológicas. Confundir infección con enfermedad instalada, o convertirla en sinónimo de incapacidad, refuerza prejuicios que durante años operaron incluso en ámbitos laborales”.
Barrera, por su parte, indicó, que la enfermedad de Chagas no se juega solo en el microscopio, en la PCR o en el laboratorio. “También se juega en los circuitos de acceso al sistema de salud, en la continuidad del seguimiento, en la posibilidad de planificar un embarazo, en la decisión de tratar a tiempo y en el modo en el que una sociedad habla de quienes conviven con esta infección”.
chagas, conicet, ihem, investigadoras, chagas congénito, chagas vectorial, ,

Desde Mendoza confirman interacción entre galaxias cercanas y su rol en la formación de estrellas
Un estudio liderado por especialistas del Conicet confirmó la interacción entre las Nubes de ...
28 DE ABRIL DE 2026
Aportes desde la ciencia al estudio del cannabis y sus derivados
La investigación científica resulta clave para comprender sus efectos, evaluar sus potencialidades ...
24 DE ABRIL DE 2026

¿Qué son los ríos atmosféricos?
Son corredores de vapor que viajan por la atmósfera y que, en zonas cordilleranas como Mendoza, ...
21 DE ABRIL DE 2026